La thyroïde est une petite glande endocrine dont le rôle est pourtant essentiel pour l’équilibre de l’organisme. Elle intervient dans la régulation du métabolisme, de la température corporelle, de l’énergie, du système cardiovasculaire et du système nerveux.
Comprendre le fonctionnement de cette glande permet d’améliorer la prise en charge naturelle des troubles thyroïdiens, qu’il s’agisse d’hypothyroïdie ou d’hyperthyroïdie.
Dans cet article, nous allons donc passer en revue les principales étapes du fonctionnement thyroïdien : la production des hormones, leur transport, leur activation et les nombreux facteurs pouvant influencer cet équilibre.
Anatomie et organisation de la thyroïde
La thyroïde est située à l’avant du cou, en avant de la trachée et de l’œsophage.
Elle est constituée de deux lobes reliés par un isthme et pèse généralement entre 25 et 30 grammes chez l’adulte.
Dans certaines situations, la glande peut augmenter de volume : on parle alors de goitre. Celui-ci peut être visible à l’œil nu ou rester discret et n’être détecté qu’à l’examen médical.
Le goitre peut apparaître :
lors d’une hypothyroïdie
lors d’une hyperthyroïdie
ou même lorsque la fonction thyroïdienne reste normale.
Il peut correspondre à un simple épaississement de la glande ou être lié à la présence de nodules.
L’axe hypothalamo-hypophysaire : le système de régulation
Le fonctionnement thyroïdien est régulé par un système hormonal appelé axe hypothalamo-hypophysaire.
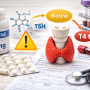
L’hypophyse sécrète une hormone appelée TSH (Thyroid Stimulating Hormone) qui stimule la thyroïde.
Sous l’action de cette hormone, la thyroïde produit deux hormones principales :
la T4 (thyroxine)
la T3 (triiodothyronine)
La T4 représente environ 80 à 90 % de la production hormonale, tandis que la T3 représente 10 à 20 %.
La T3 est l’hormone réellement active au niveau cellulaire.
La T4 agit essentiellement comme une hormone de réserve, qui devra être convertie en T3 dans différents tissus de l’organisme.
L’axe hypothalamo-hypophysaire fonctionne selon un mécanisme de rétrocontrôle : lorsque les concentrations de T3 et T4 sont suffisantes, la production de TSH diminue ; lorsqu’elles sont trop faibles, la TSH augmente afin de stimuler la thyroïde.
Transport des hormones thyroïdiennes
Une fois libérées dans la circulation sanguine, les hormones thyroïdiennes ne circulent pas seules.
Elles se lient à des protéines de transport, principalement :
la TBG (thyroxine binding globulin)
la transthyrétine
l’albumine
La TBG est la principale protéine de transport et assure la fixation d’environ :
70 % de la T4
63 % de la T3
Lorsque les hormones thyroïdiennes sont liées à ces protéines, elles sont inactives.
Seule la fraction libre peut agir sur les cellules.
Certaines situations hormonales peuvent modifier ce système de transport.
Par exemple, une dominance en œstrogènes peut augmenter la production de TBG et ainsi réduire la fraction d’hormones thyroïdiennes disponibles pour les cellules.
Comment la thyroïde fabrique ses hormones
La thyroïde est constituée de nombreuses petites structures appelées follicules.
Ces follicules sont composés de cellules spécialisées appelées thyréocytes, qui produisent une protéine appelée thyroglobuline.
La thyroglobuline est riche en tyrosine, un acide aminé indispensable à la fabrication des hormones thyroïdiennes.
La synthèse des hormones thyroïdiennes nécessite deux éléments principaux :
l’iode
la tyrosine
L’iode est capté par les thyréocytes sous forme d’iodure à partir du sang.
Une enzyme clé intervient ensuite dans la fabrication des hormones : la thyroperoxydase (TPO).
Cette enzyme permet l’iodation de la tyrosine et la formation des hormones thyroïdiennes.
Les cofacteurs nécessaires à la synthèse hormonale
La production des hormones thyroïdiennes dépend également de nombreux cofacteurs.
Parmi les plus importants :
fer
zinc
sélénium
magnésium
vitamines A, B6 et B9
Une carence dans ces nutriments peut perturber la production hormonale.
Conversion de la T4 en T3
Comme nous l’avons vu, la majorité des hormones produites par la thyroïde est constituée de T4.
Cette hormone doit être transformée en T3 active.
Cette conversion est assurée par une enzyme appelée 5-désiodase.
Elle se déroule principalement dans :
le foie
les reins
les intestins
les muscles
le cerveau
Le microbiote intestinal participe également à cette conversion, ce qui explique pourquoi les déséquilibres digestifs peuvent influencer la fonction thyroïdienne.
La T3 reverse : un mécanisme d’adaptation
Dans certaines conditions, la T4 peut être convertie en T3 reverse (rT3).
Cette forme hormonale est inactive.
Une production excessive de rT3 peut ralentir le métabolisme.
Ce phénomène apparaît notamment lors :
de jeûne prolongé
de stress important
d’infections
d’inflammation chronique
de certaines maladies hépatiques
ou lors d’un excès de cortisol.
Il s’agit d’un mécanisme d’adaptation permettant à l’organisme de réduire sa dépense énergétique.
Le rôle du foie et du microbiote
Le foie joue un rôle essentiel dans la conversion de la T4 en T3.
Il participe également à la production des protéines de transport des hormones thyroïdiennes.
Le microbiote intestinal intervient aussi dans la transformation hormonale grâce à certaines enzymes bactériennes.
Un déséquilibre du microbiote peut donc perturber la régulation thyroïdienne.
L’influence du stress
Le stress chronique influence fortement la fonction thyroïdienne.
Une augmentation prolongée du cortisol peut :
inhiber la production de TSH
diminuer la conversion de T4 en T3
augmenter la production de T3 reverse.
Ces mécanismes peuvent contribuer à l’apparition d’un ralentissement thyroïdien fonctionnel.
Les anticorps antithyroïdiens
Certaines pathologies thyroïdiennes sont d’origine auto-immune.
Dans ces situations, l’organisme produit des anticorps dirigés contre la thyroïde.
Les principaux anticorps sont :
anticorps anti-TPO
anticorps anti-thyroglobuline
anticorps anti-récepteurs de la TSH (TRAK)
Les anticorps anti-TPO sont les plus fréquemment retrouvés dans la thyroïdite de Hashimoto.
Les anticorps TRAK sont caractéristiques de la maladie de Basedow, où ils stimulent excessivement la thyroïde.
Ce qu’il faut retenir
Le fonctionnement thyroïdien dépend d’un équilibre complexe impliquant :
l’axe hypothalamo-hypophysaire
la production hormonale par la thyroïde
le transport sanguin des hormones
leur conversion dans différents organes
l’état nutritionnel
le microbiote
et l’équilibre hormonal global.
Comprendre ces interactions permet d’améliorer la prise en charge des troubles thyroïdiens dans une approche intégrative.
Voilà pour les infos du jour,
Et pour ne pas manquer les prochains articles du blog, inscrivez vous à la newsletter ;-)
Véronique




Bonjour Véronique,
j’ai découvert que j’avais une hyperthyroïdie en sept 2021, avec la maladie de Basedow. Mes dernières analyses montraient que j’avais une t3 à 4.6 et t4 à 2.2 et TSH toujours à zéro. Mes prochaines analyses seront le 20 juin. Les tracks étaient il y a 2 mois à 9.2. Je prends du néo mercazole 15mg, mais aussi de la gemmo de cassis pour calmer l’inflammation des tissus orbitaires et j’ai une légère exophtalmie. Le plus dur pour moi est l’impression de “perde mes neurones” , le brouillard mental qui est accompagné de bcp d’angoisses. Je suis quasi en permanence angoissée et j’essaie de gérer par l’action. Je prends aussi de leffexor 150mg et voudrais bien arrêter au plus vite. Je me fais aussi suivre par un acuponcteur. Il y a 3 jours j’ai commencé un protocole Biofirm de chez Biophoenix pour nettoyer mes intestins et l’homéopathe qui me suit me dit que cela devrait aller bcp mieux d’ici septembre. Que me recommanderiezvous pour ces angoisses. Je ne suis pas sûre que cela fasse partie des symptômes de la maladie de Basedow,… Ces angoisses/cerveau embrouillé sont vraiment difficiles à vivre. J’ai 51 ans et suis célibataire et traverser cela en vivant seule m’est difficile même si j’ai des amis proches et famille. Merci d’avance. Peut être puis je vous appeler ?
Merci d’avance de votre retour
Soazig
Bonjour Soazig, oui, appelez moi, et nous échangerons quelques instants…Je vous donnerai quelques pistes..
Bien à vous